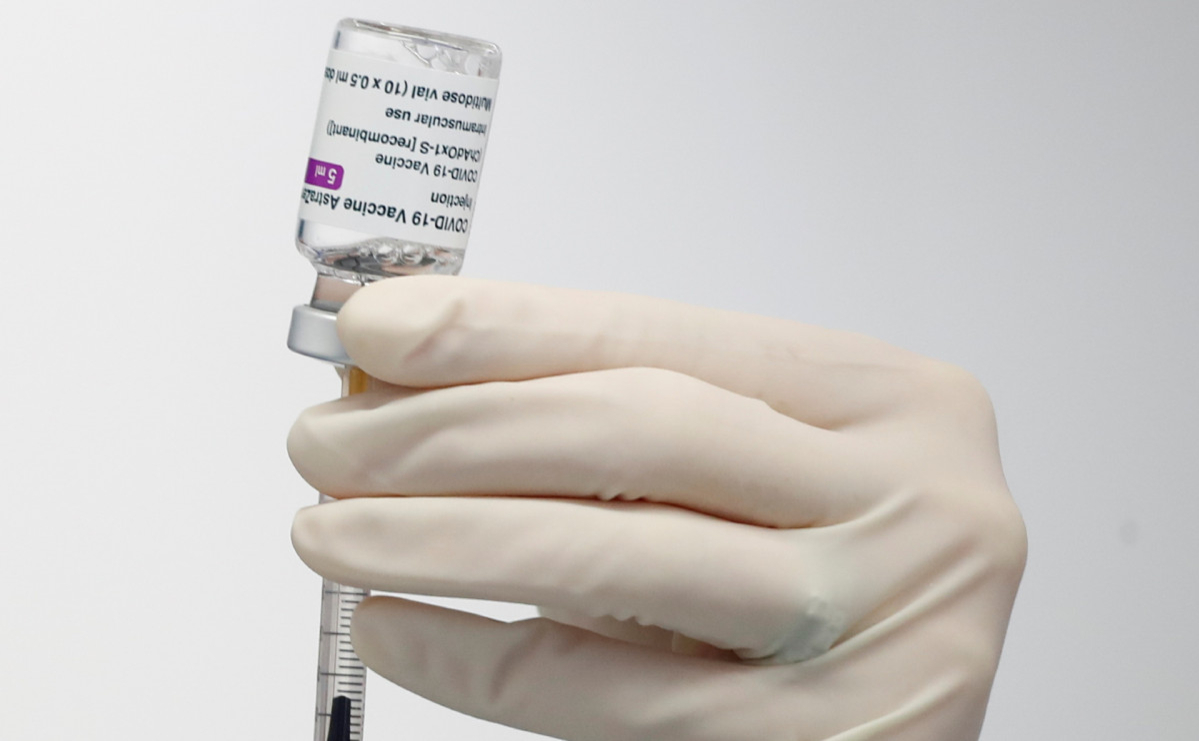
СМИ узнали об отказе от испытаний связки «Спутника V» с AstraZeneca
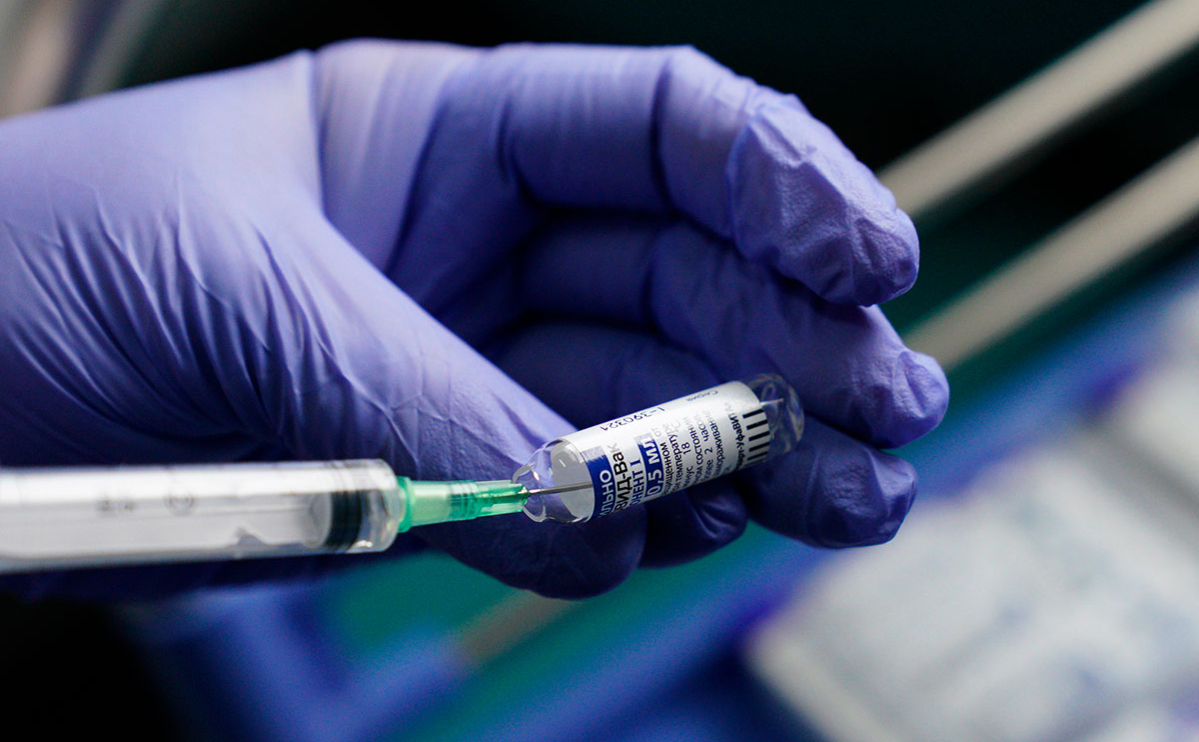
Этический комитет Минздрава не одобрил проведение клинических испытаний комбинации вакцин от коронавируса AstraZeneca и «Спутник V», сообщил «Фармвестник».
В своем материале «Фармвестник» ссылается на документ, в котором говорится о первой и второй фазах испытаний комбинации вакцин AZD1222 и rAd26-S на взрослых.
Вакцина AstraZeneca также называется AZD1222 в промежуточном отчете компании о клиническом исследовании I—II и III фаз, такая же кодировка есть в реестре разрешенных клинических исследований Минздрава, выяснило издание. rAd26-S, по его информации, — это аббревиатура первого компонента «Спутника V», которая содержит вектор на основе аденовируса 26-го типа. Такое же обозначение использовалось в публикации отчетов о клинических исследованиях «Спутник V» в медицинском журнале The Lancet.
Кроме того, кодировка самого исследования D8111C00003, указанная в документе, совпадает с данными об испытаниях, опубликованными в международном реестре clinicaltrials.gov. Из записи этого реестра следует, что инъекцию должны были получить две группы добровольцев. Первая получит сначала инъекцию вакцины AZD1222, а на 29-1 день после этого — первый компонент «Спутника V» (rAd26-S). В другой группе вакцинацию проведут в другом порядке.
По данным из реестра, исследование планировалось в Белоруссии и шести центрах в России. Спонсором исследования в реестре указана AstraZeneca, соавторами — компания «Р-Фарм», Российский фонд прямых инвестиций (РФПИ) и разработавший «Спутник V» Центр им. Гамалеи.
В AstraZeneca сообщили РБК, что пока компания не получила официального подтверждения от комитета по этике о решении в отношении исследования. «Данная информация не означает, что исследование не одобрено. Вопросы, заданные комитетом по этике, имеют отношение к первоначально поданным документам. Нам поступил запрос от Министерства здравоохранения РФ о предоставлении дополнительных данных в рамках процесса одобрения исследования. Мы готовим обновленный пакет документов и планируем направить его в Минздрав в ближайшее время», — заявили в компании.
В Центре им. Гамалеи отказались от комментариев. РБК направил запрос в Минздрав.
Создатели «Спутника V» предложили AstraZeneca провести совместные испытания препаратов в ноябре прошлого года. Они напомнили, что испытания, при которых добровольцы получали полную дозу вакцины AstraZeneca, показали эффективность 62%. «Если они пойдут на новое клиническое испытание, мы предлагаем попробовать режим комбинирования вакцины AstraZeneca со «Спутником V», чтобы повысить эффективность. Комбинированные вакцины могут стать важными для ревакцинации», — заявили создатели российской вакцины. В декабре AstraZeneca анонсировала начало совместных испытаний комбинации вакцин. В январе владелец «Р-Фарма» Алексей Репик говорил Reuters, что исследования начнутся в феврале и пройдут в Азербайджане, Аргентине, Саудовской Аравии, ОАЭ, Белоруссии, России и других странах.
В начале весны ряд европейских стран приостановили вакцинацию препаратом AstraZeneca. Поводом стали сообщения о редких случаях образования тромбов и нарушения свертываемости крови у привившихся и нескольких смертях. В самой компании заявили, что вакцина соответствует всем критериям безопасности.
В европейском лекарственном регуляторе подчеркивали, что положительный эффект от препарата превышает возможные риски побочных реакций. Всемирная организация здравоохранения также рекомендовала продолжить использование вакцины AstraZeneca. В ней связи между вакцинацией препаратом AstraZeneca и образованием тромбов пока не нашли.